主要的生物低温保存方法是慢冻、快速玻璃化和低温储存。每种方法都有其独特的局限性:
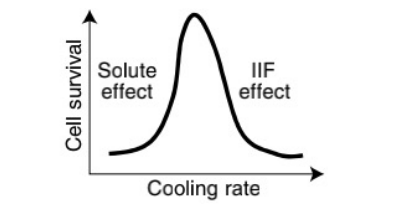
● 慢速冷冻:需要针对细胞类型的特定冷却速率,以最小化冰形成和脱水。
● 玻璃化冷冻:需要高浓度的冷冻保护剂和小样本体积。
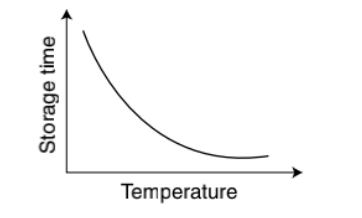
● 低温储存:较高温度限制保存时间。
生物样本遵循热力学路径缓慢降温期间冰晶形成并扩展和生长
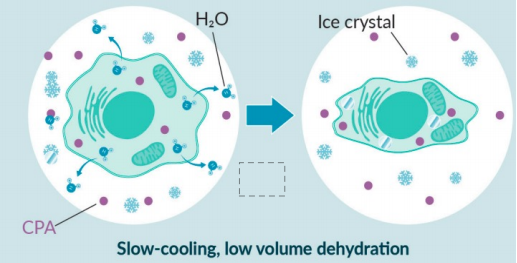
~ 10⁰℃/分钟; -80 - -193 ℃
局限性: 外围细胞脱水过度,核心细胞脱水不足 产生冰晶,撕裂细胞膜并导致细胞死亡

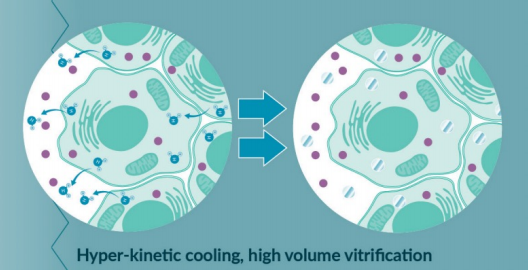
在非冻结温度下装入高浓度的CPA通过快速非平衡冷却过程实现玻璃化
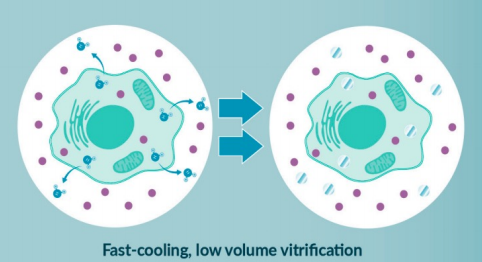
> 10²℃/分钟; -80 - -193 ℃
局限性: 高浓度的冷冻保护液产生剧毒物质 效率较低
贮存温度高于平衡冰点线
~ 10⁻¹℃/分钟; 0 - 4 ℃
局限性: 产生缺血性损伤 保存时间短
● 针对冷冻保存技术现存在的缺陷,目前公司的研究主要包含"预脱水+植冰""局部玻璃化"以及"深度过冷保存"等技术方向,通过降低冻存溶液毒性、抑制冰晶形成、控制冰晶形成位置等方式提高细胞、组织、器官保存的可靠性和安全性。
| 技术原理 | 效果 | |
|---|---|---|
| 预脱水+植冰 | ■ 使用细胞外海藻糖将细胞预脱水至最小体积,最小化渗透活性 ■ 在零度以下高温(>10℃)诱导冰晶形成(即植冰) |
✓ 避免使用传统的有毒透膜冷冻保护剂(pCPA) ✓ 成纤维细胞、成体干细胞和红细胞在冷冻保存后无需pCPA即可实现高细胞活力或恢复 |
| 局部玻璃化 | ■ 对器官或组织的某些关键部位(如血管或细胞密集区域)进行玻璃化处理,而不需要整个组织完全玻璃化 | ✓ 采用较低浓度的防冻剂,以减少毒性,同时通过快速冷却,使特定区域达到玻璃化状态,从而减少冰晶形成和冷冻损伤。 ✓ 用于保存较大的器官和复杂组织,如肝脏和心脏 |
| 深度过冷保存 | ■ 用矿物油等不与水混合的溶液覆盖表面,阻断水和空气之间的界面 ■ 使器官在零下温度而不结冰的状态下保存,防止水分在细胞内外形成冰晶 |
✓ 可显著降低器官保存温度,延长器官的保存时间并减少损伤 ✓ 实验表明,使用这种技术可以将肝脏的保存时间从传统的6-12小时延长至24小时以上,极大地提高了器官移植的成功率和应用范围 |
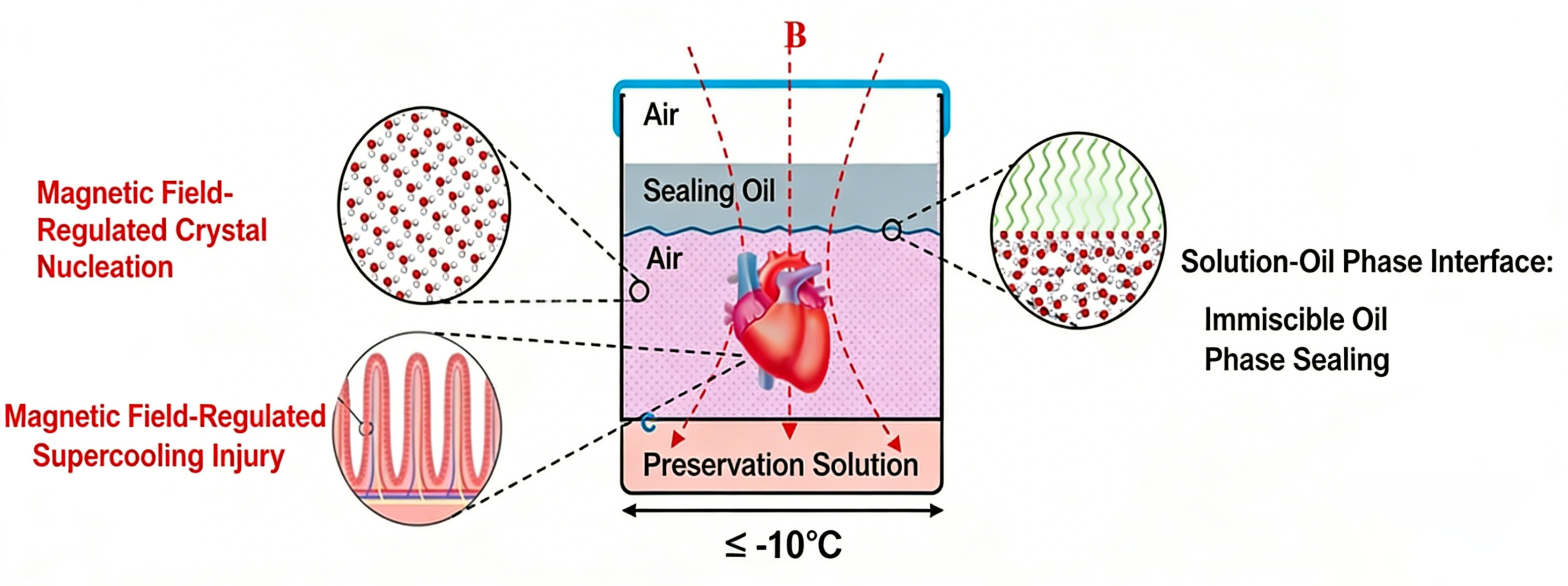
CryoPreserve 平台将非侵入性磁场物理调控技术与油封界面隔离技术深度融合,突破传统器官保存的温度瓶颈,将器官保存温度拓展至 - 10℃以下,实现器官在亚稳态下的长期、稳定、无损伤保存,为器官移植领域带来革命性突破。
传统器官保存受限于 0-4℃的安全温度区间,保存时长短、器官损伤风险高,严重限制移植手术的可及性。CryoPreserve 平台以深度过冷保存为核心技术,通过磁场物理调控与油封界面隔离的双协同策略,在 - 10℃以下的亚稳态环境中,实现器官的无冰晶、低氧化应激稳定保存,大幅延长器官保存时限,降低移植后器官功能损伤。
针对传统器官保存中冰晶损伤与代谢衰变不可调和的矛盾,本平台创新性提出基于磁场调控的深度过冷保存技术。通过大幅拓展器官安全保存温度区间至 - 10℃以下,显著延缓器官代谢与功能衰败速率,有效延长离体器官保存时限,为临床器官移植提供颠覆性技术支撑。
采用磁场 + 油封双重非侵入式物理调控方案,全程无需引入外源化学保护剂,从根源上避免化学干预带来的细胞毒性与副作用,开创器官 "纯物理保护" 全新路径。系统解析器官保存体系(保存液、细胞及组织)冰晶成核关键位点与生长机制,结合界面油封隔离与外场精准加载,抑制器官内外晶核形成与冰晶生长,构建稳定深度过冷状态,实现更低温度下的安全保存。
通过阐明磁场调控对器官过冷损伤的分子与细胞机制,系统性降低器官在深度过冷保存过程中的氧化应激水平与细胞凋亡率,多靶点协同保护细胞结构与生理功能,显著提升器官保存质量与移植后功能恢复效果。
本平台专用保存液以器官生理稳态维持与能量供给为核心功能,配方严格遵循生理环境设计,为离体器官提供稳定的离子环境、渗透压调控及基础代谢能量底物,保障器官在低温状态下的基本生命活动。产品不添加抗冻剂及其他外源性化学保护成分,完全依托磁场与油封构成的纯物理保护体系实现深度过冷稳定,避免化学试剂对器官造成的二次损伤,实现真正意义上的无创、温和保存。
设备集成精准低温控制、非侵入性磁场加载与油封界面调控于一体,可稳定实现 - 10℃以下深度过冷环境。通过物理场协同作用抑制冰晶成核、削弱冰晶生长驱动力,无需依赖抗冻剂即可构建稳定亚稳态保存体系,同时支持实时温度、场强等关键参数监测,兼顾器官转运安全与操作便捷性,为器官长途保存与临床移植转运提供可靠硬件支撑。
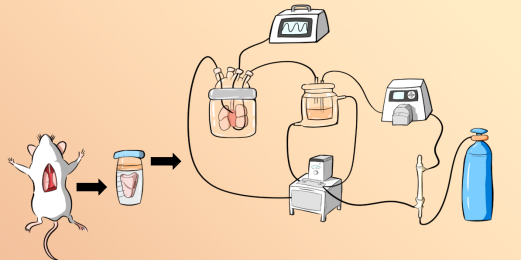
针对心脏高代谢、易缺血损伤的特点,采用深度过冷 + 纯物理保护方案,将心脏保存温度拓展至 - 10℃以下,显著延缓心肌代谢衰退。在无抗冻剂添加的前提下,通过磁场抑制冰晶形成、降低氧化应激,配合油封界面稳定过冷体系,最大限度保护心肌细胞结构与收缩功能,有效延长心脏安全保存窗口,提升移植后器官功能恢复率与手术成功率。全流程标准化:从供体获取、灌流保存到转运、移植,提供完整标准化操作流程
| 产品/技术名称 | 核心目标/技术 | 应用场景 | 开发阶段 | 预计时间 |
|---|---|---|---|---|
| CryoSafe-HSCTM 血液干细胞冷冻保存溶液 | 复合配方,高浓度玻璃化,风险消除 | 造血干细胞 | 已上市 | / |
| CryoSafe-UB™ 脐带血冷冻保存液 | 复合配方,高浓度玻璃化冷冻,风险消除 | 脐带血细胞 | 临床前验证 | 2027-2028 |
| CryoSafe-MSCTM 脐带来源间充质干细胞低温保存液 | 复合配方,高浓度玻璃化冷冻,风险消除 | 脐带间充质干细胞 | 临床前验证 | 2027-2028 |
| CryoSolv-H™ 心脏保存液 | 能量供应 + 抗氧化保护 | 心脏保存 | 临床试验 | 2026-2027 |
| CryoChamber-I 便携式保存舱 | 非侵入式磁场 + 精确温度控制 | 器官运输与保存 | 临床前验证 | 2026-2027 |
| HeartPreserve™ 集成心脏保存溶液 | 磁场 + 油封 + 保存液集成 | 全心移植工作流程 | 优化阶段 | 2027-2028 |